それぞれの濃度は,密度やモル質量などを使って,濃度の変換をすることができる。 濃度の変換問題は,質量パーセント濃度% ⇔ モル濃度mol/L の変換が頻出となる。 Ⅰ質量パーセント濃度に関する問題タイプ Ⅱモル濃度に関する問題タイプ濃度を計算する問題 2組の入口へ 説明へGO 1 水酸化ナトリウムの結晶gを水80gに溶解させ、水酸化ナトリウム水溶液を作る。この水溶液の密度を12g/cm 3 とするとき、以の濃度を求めよ。 (原子量H=10,O=16,Na=23) 1,質量パーセント濃度 2,モル濃度 質量パーセント濃度を求めるには、公式にあてはめれば一瞬。 質量パーセント濃度は 15% でした。 食塩水が100gあれば、その中に15gの食塩が溶けているくらいの濃さ、ってことです。

モル濃度1 0mol Lの過酸化水素水 密度1 2g Cm の質量パーセント濃度 Clear
質量 パーセント 濃度 密度
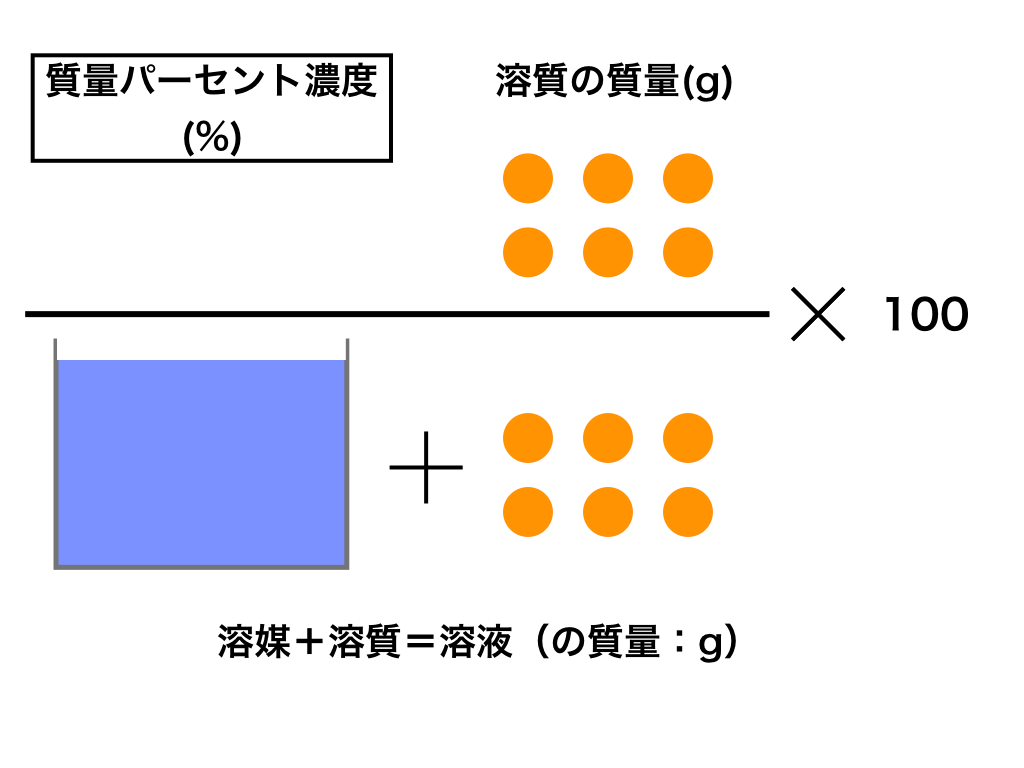
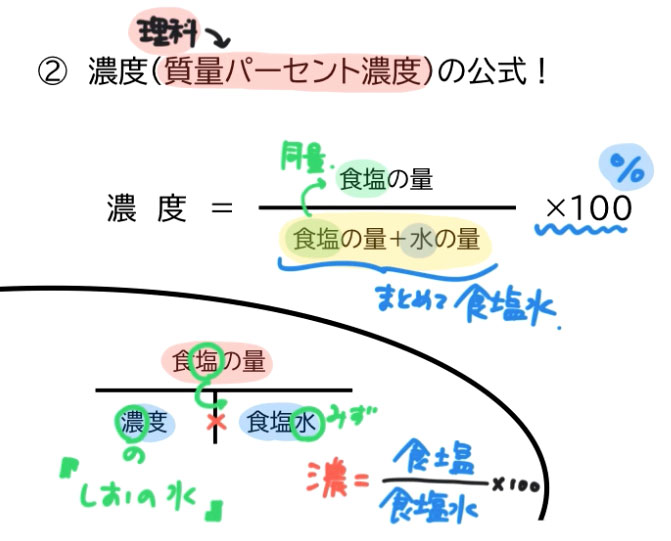
質量 パーセント 濃度 密度- 化学 質量パーセント濃度・・・! 問1、密度0195g/mLの塩化ナトリウム水溶液100mL中に含まれている塩化ナトリウムが、702g質量パーセント濃度 質量パーセント濃度(%)= 溶質の質量(g) 溶液の質量(g) ×100 例 90gの水に10gの塩化ナトリウムをとかしたら、 100gの塩化ナトリウム水溶液になる。 このとき 溶質10g, 溶液(溶媒溶質)100gなので 濃度は




090g Cm3 Descubre Como Resolverlo En Qanda
それぞれの濃度の変換と密度 (from)質量パーセント濃度から→(to)mol濃度 解答編:質量%→mol濃度 (from)質量パーセント濃度→(to)質量モル濃度へ 解答編動画一覧や問題のプリントアウトはこちらをご利用ください。ホームページ → http//19chtv/ Twitter→ https//twittercom/haichi_toaru質量パーセント濃度が 22% 、密度が 12g/mL の水酸化ナトリウム水溶液があります。 この水溶液の モル濃度 を求めていきましょう。 さて、どのようにしてモル濃度を求めるか、イメージできますか? 最初に注目するのは、 単位 です。 密度の単位は、「g/mL」です。 モル濃度の単位は、「mol/L」です。 「g/mL」 を 「mol/L」 に変換していくイメージですね。 計算の
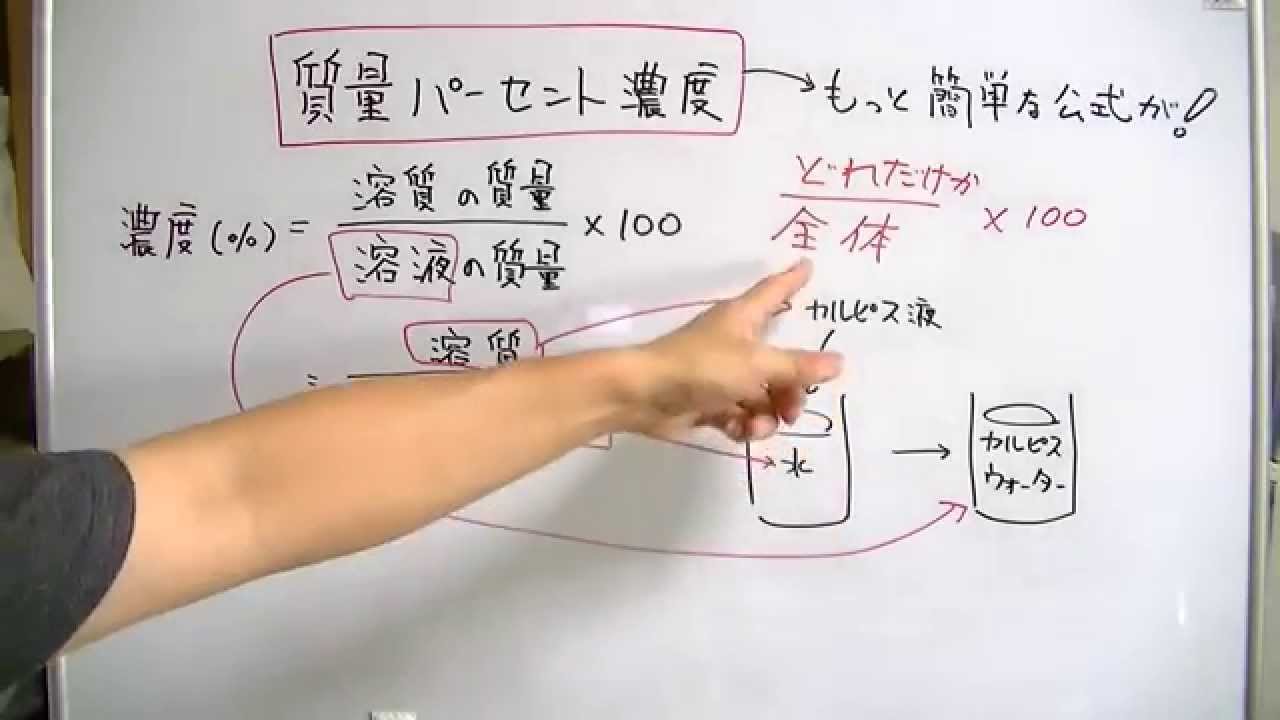
質量パーセント濃度の求め方の公式は、 (質量パーセント濃度 % )= (溶質の質量)÷(溶液の質量)×100質量パーセント濃度 をどのように求めるかというと、次の式に当てはめます。 質量パーセント濃度〔%〕= (溶質の質量〔g〕/溶液の質量〔g〕)×100その密度が12g/mlであるから、溶液の質量は10gである。 質量パーセント濃度が37%であるから溶液に溶け込んでいる塩酸の質量は10*37%=444gとなる。 HCLの分子量が365であるからそのモル質量も365g/molとなる。 従って、HCLの量は444/365=122mol
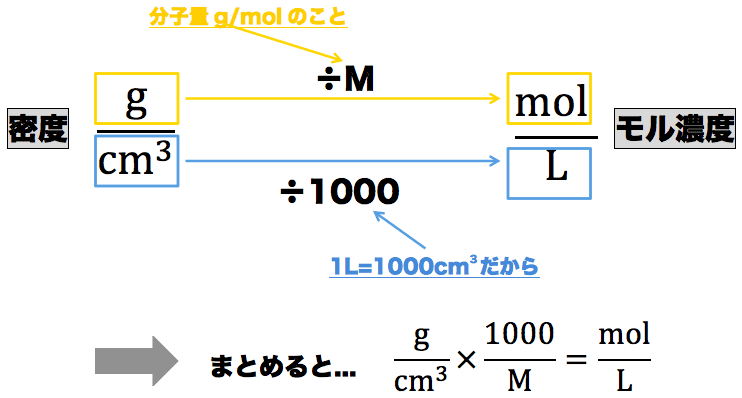
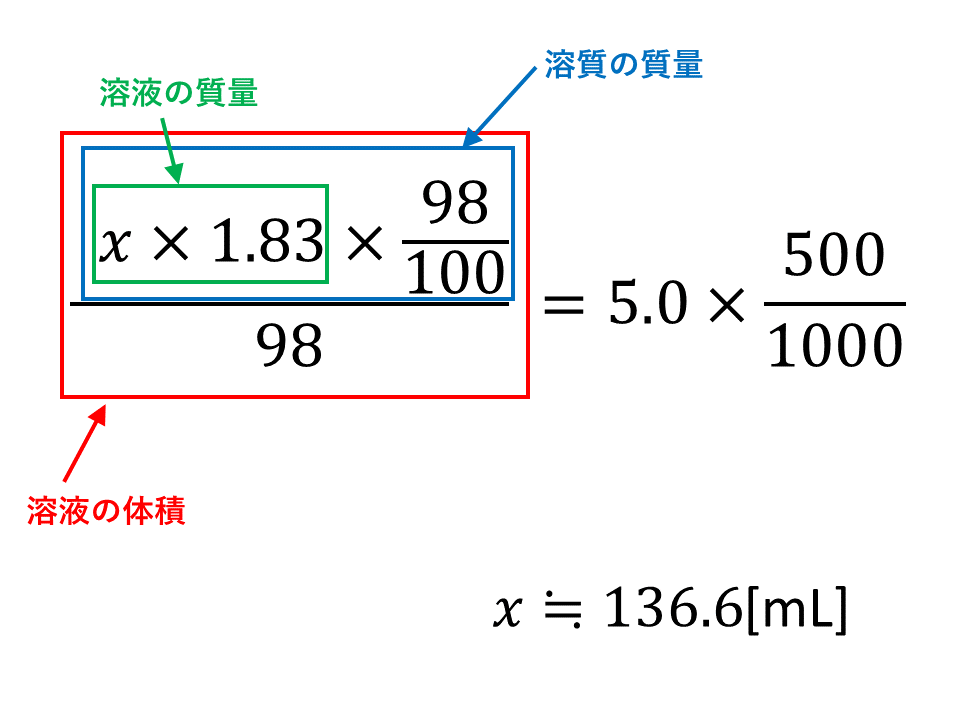
ふつうに「濃度」といえば質量濃度。 モル濃度は 1リットル中の mol 数。 この定義の違いを理解していれば換算できるはず。 ① 「濃度98%濃硫酸」1リットルの質量は 18 g/cm^3 × 1000 cm^3 = 1800 g そのうち「硫酸」は 98% なのだから、硫酸の質量は 1800 gかなり間があいてしまいましたが、前回の解説をしていきます。先ずは、質量パーセント濃度と密度か ら、モル濃度を求めることから始めましょう。 一般に、溶質の分子量(式量)を\\(M\\) , 溶液の密 続いて、この塩化ナトリウム水溶液に13gの塩化ナトリウムが含まれているときの 質量パーセント濃度を求めます。 質量パーセント濃度は、 (溶質の質量/溶液の質量)×100 ※溶液=溶媒溶質 で求められます。



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



受験化学 9 溶解度の計算1 みかみの参考書ブログ
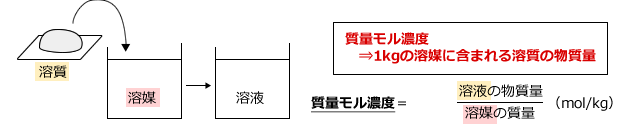
「質量パーセント濃度」という場合は溶液(均一な混合物)について質量パーセントで表した濃度ということになります。 質量パーセント濃度=(溶質の質量/溶液の質量)×100 (溶液の質量=溶質の質量+溶媒の質量) です。溶質の質量g 溶液の質量g ×100 で表す。 w/v% は,質量体積パーセント濃度,若しくは質量容積パーセント濃度といい,分子が溶質 の質量 gで分母が溶液の体積mL の場合であり,w/v% = 溶質の質量g 溶液の体積mL ×100 で表す。 v/v% は,体積パーセント濃度と溶液の密度がわかれば質量パーセント濃度との変換 が行なえる。 式1 分子量(モル質量)M の物質の質量パーセント 濃度a%の溶液のモル濃度。密度はd(g/mL)。 ④ 質量モル濃度(molality) 溶媒1kg に溶けている溶質の量を物質量(mol)で 表した濃度。




密度や質量パーセント濃度の計算の 覚え方を教えてください Clear
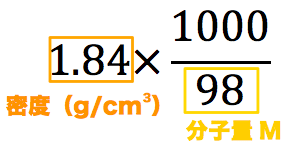



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ
質量パーセント濃度98%、密度184g/cm 3 の濃硫酸(分子量98)のモル濃度を求めよ。 とりあえず密度と分子量を使って計算式を立てる。 基本これを計算すれば終了だが、今回は 質量パーセント濃度の記載があるのでそれを掛ける。 水溶液は「質量パーセント濃度の求め方」、 状態変化は「水の状態変化」を押さえておけばいいんじゃないかな! 帰国子女(男子) より 18年2月16日 442 AM(1) 質量パーセント濃度 質量パーセント濃度は、溶液の質量にたいして溶質の質量がどれくらい含まれているかを表すもので、100gの溶液中に含まれる溶質の質量(g)を表します。 (2) (体積)モル濃度




高校理論化学 溶液の濃度と調製 質量パーセント濃度 密度とモル濃度の単位換算 受験の月
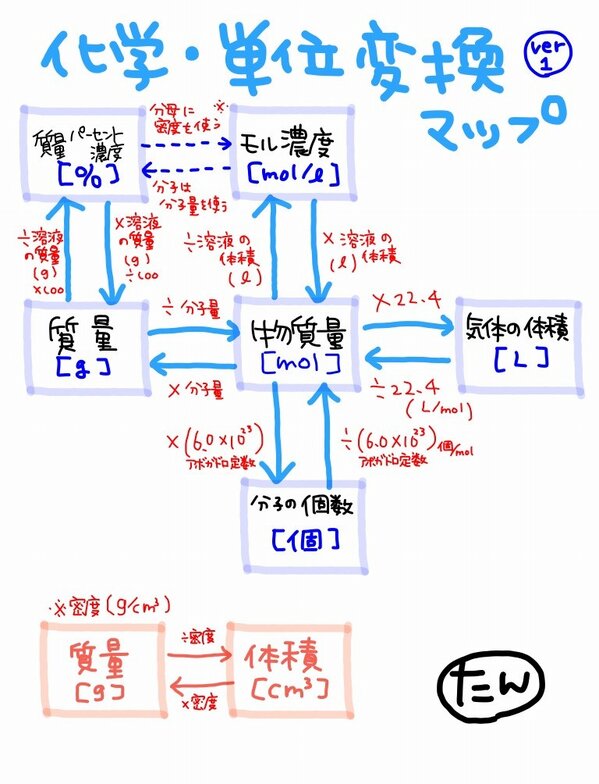



たんくん على تويتر 教えた覚えあるよー その時はモル濃度と質量パーセント濃度は別やったけどな これは少し無理やりつけた感がある Rt Hanpen52 おお 懐かしい こんなの昔頭の中にありましたね
パーセント濃度は、溶質の質量÷溶液の質量×100です。<数式の挿入> ②で求めた溶質の質量÷①で求めた溶液の質量×100で求められるので、<数式の挿入> 438 ÷ 10 ×100= 365% <数式の挿入> これより、求める質量パーセント濃度は365%となります。3年以上前 はてなさん 質量パーセント濃度が25%の食塩水の密度を求めなさい。 水の密度は10g/㎠として、水に食塩を溶かしても体積は変化しないものとする。 答えは少数第二位を四捨五入して、小数第一位まで答えなさい。 この問題の解き方を詳しく教えてください! ! 質量パーセント濃度 密度 濃度 理科 中学モル濃度10mol/Lの過酸化水素水 (密度12g/cm³)の質量パーセント濃度 Clear 化学




化学 6回目授業 ブログ De 授業 21




138 Descubre Como Resolverlo En Qanda
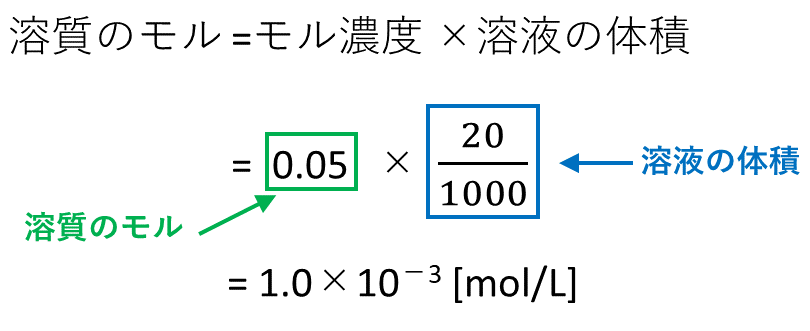
この砂糖水の質量パーセント濃度は何%か。 (3) 100gの水に60gの砂糖を入れてつくった砂糖水の質量パーセント濃度は何%か。 次の問いに答えよ。 (1) 質量パーセント濃度4%の塩化ナトリウム水溶液を250g作る場合 塩化ナトリウムは少なくとも何g必要か。 モル濃度と質量パーセント濃度の計算(問題と答え) 原子量:H=1, C=12, N=14, O=16, Na=23, Cl=355, S=32, Cu=64 ①水酸化ナトリウム16gを水に溶かしてLにしたときの濃度は何mol/Lか。 ②塩化水素56L(標準状態で)を水に溶かして全体を100mLにした。 モル濃度マスターへの道! ① もし物質 (mol)が分からなければ、物質量に変換してから溶液の体積 Lで割りましょう。 では今回は、モル濃度の問題の中でも密度が与えられて 「モル濃度から質量パーセント濃度へ変換せよ」 という問題について一緒に




6 7 モル濃度と密度から質量パーセント濃度を計算します 1lあったとしたら と仮定すれば あとは簡単です プレテスト化学基礎 第3問 問3 Youtube




4 6 溶液の濃度 おのれー Note
密度 118g/cm 3 から溶液 1L の質量(g)は 118g/cm 3 = 118g/mL = 1180g/L となり、問題文の塩酸は 1L で 1180g とわかりました。 (4) 最後に質量パーセント濃度(%)を求めましょう。 質量パーセント濃度(%)= 溶質の質量(g)÷ 溶液(溶質溶媒)の質量(g)×100なので、 質量パーセント濃度3 (%を求める) (8問) 0点 質量パーセント濃度を求めよ。 (割り切れない場合、小数第1位で四捨五入せよ) ある濃度の水溶液A300gに水0gを混ぜると濃度18%の水溶液B500gができた。 このときのもとの水溶液Aの濃度。 解答解説 × ある濃度の質量パーセント濃度と容量モル濃度 7 市販の濃硝酸は600%のHNO3 の水溶液で、密度が136 g/cm 3 濃度が400%の希硫酸の密度は130 g/cm3 である。この希硫酸の容量モル濃度はいくらか。有効数




質量パーセント濃度 塾の質問箱




質量パーセント濃度に関する問題です 0 4がどこから出てきたのかわかりません Clear




世界一雑な高校化学動画 モル濃度と質量パーセント濃度 Skmkchem Youtube



10倍に薄める前の食酢中に含まれる酢酸のモル濃度と質量パーセント濃度はいく Yahoo 知恵袋



5分でわかる モル濃度と密度 質量パーセント濃度の考え方を図と練習問題付きで徹底解説 サイエンスストック 高校化学をアニメーションで理解する




溶液の濃度 問題8 体積加算性の無い液体の混合 Youtube
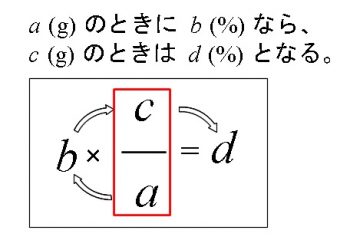



溶液の質量パーセント濃度の求め方と比重を利用した計算問題




92 Descubre Como Resolverlo En Qanda




なぜ密度をかけないのでしょうか0 50lになる理由をお願いします Clear
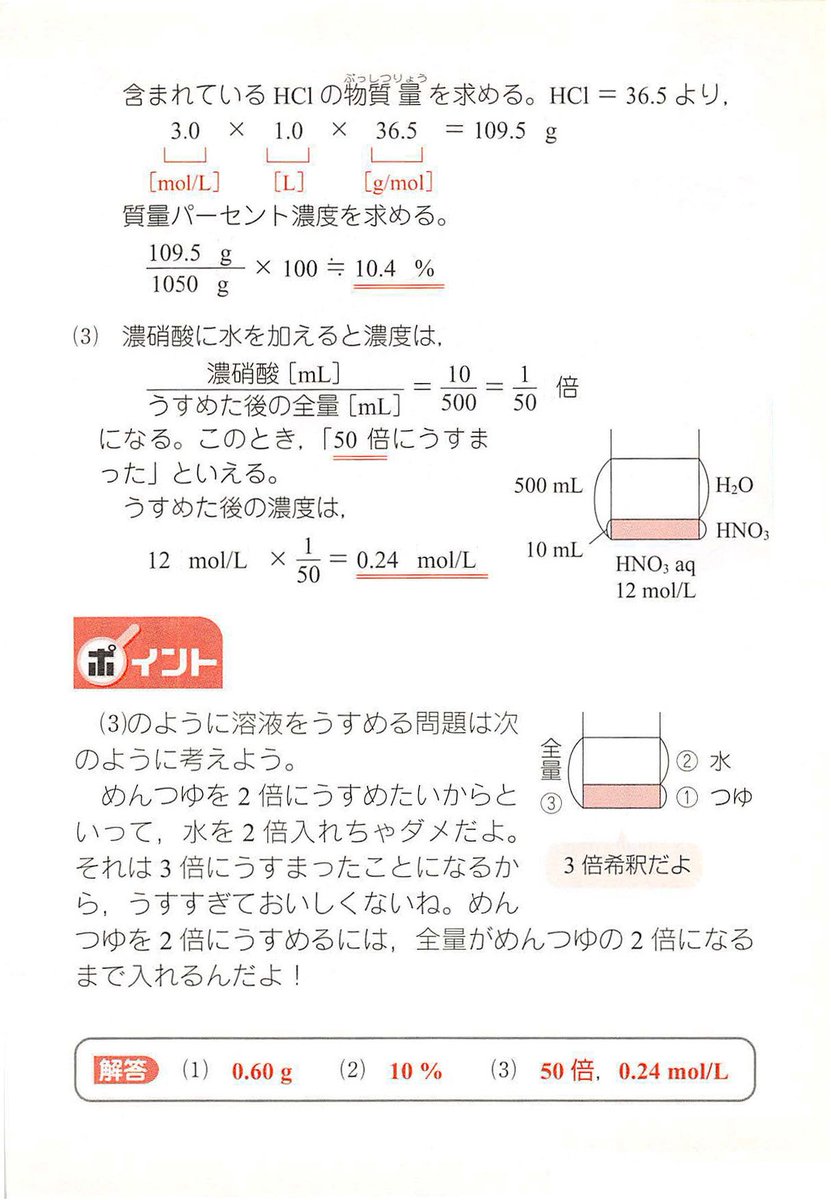



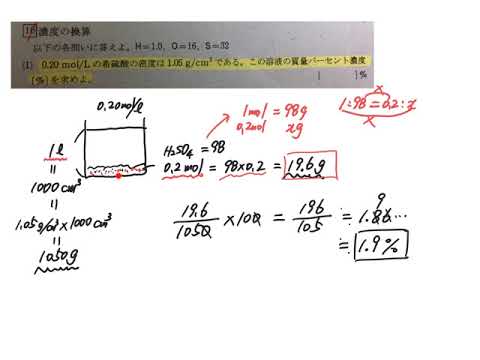
西村能一 科学の名著50冊が1冊でざっと学べる Kadokawa 化学計算問題 6 濃度 G Mol Lを求める 1 0 10 Mol L酢酸ch Cooh水溶液100 Mlに酢酸は何g溶けているか 2 3 0 Mol Lの塩酸 密度1 05g Cm の 質量パーセント濃度は何 か 3 12




1 0moll 105gcm3 See How To Solve It At Qanda




西村能一 科学の名著50冊が1冊でざっと学べる Kadokawa 化学計算問題 6 濃度 G Mol Lを求める 1 0 10 Mol L酢酸ch Cooh水溶液100 Mlに酢酸は何g溶けているか 2 3 0 Mol Lの塩酸 密度1 05g Cm の 質量パーセント濃度は何 か 3 12




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット




高校化学 質量モル濃度 映像授業のtry It トライイット




モル濃度から質量パーセント濃度 Twitter Search Twitter
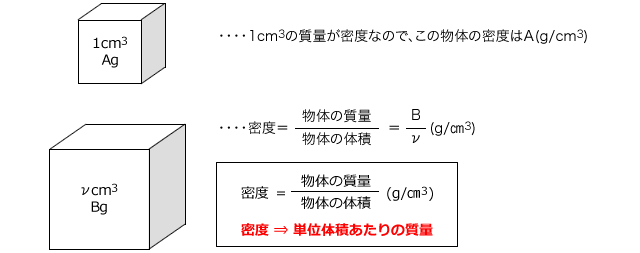



化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム




質量パーセント濃度と密度の意味的な違いって何ですか 96の 2 がよ 化学 教えて Goo




質量パーセント濃度の求め方とモル濃度の違い
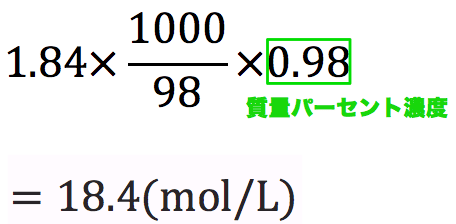



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ



問題 食酢中の酢酸の質量パーセント濃度として 最も適当な数値を選べ ただし Yahoo 知恵袋




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ



化学 質量パーセント濃度が80 0 の硫酸水溶液を水で希釈し Yahoo 知恵袋




4 6 溶液の濃度 おのれー Note




高校化学基礎 濃度 密度を用いた質量パーセント濃度とモル濃度の変換 Youtube




0mola C6h12o6 Descubre Como Resolverlo En Qanda




090g Cm3 Descubre Como Resolverlo En Qanda
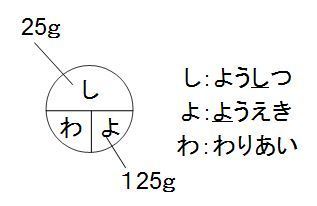



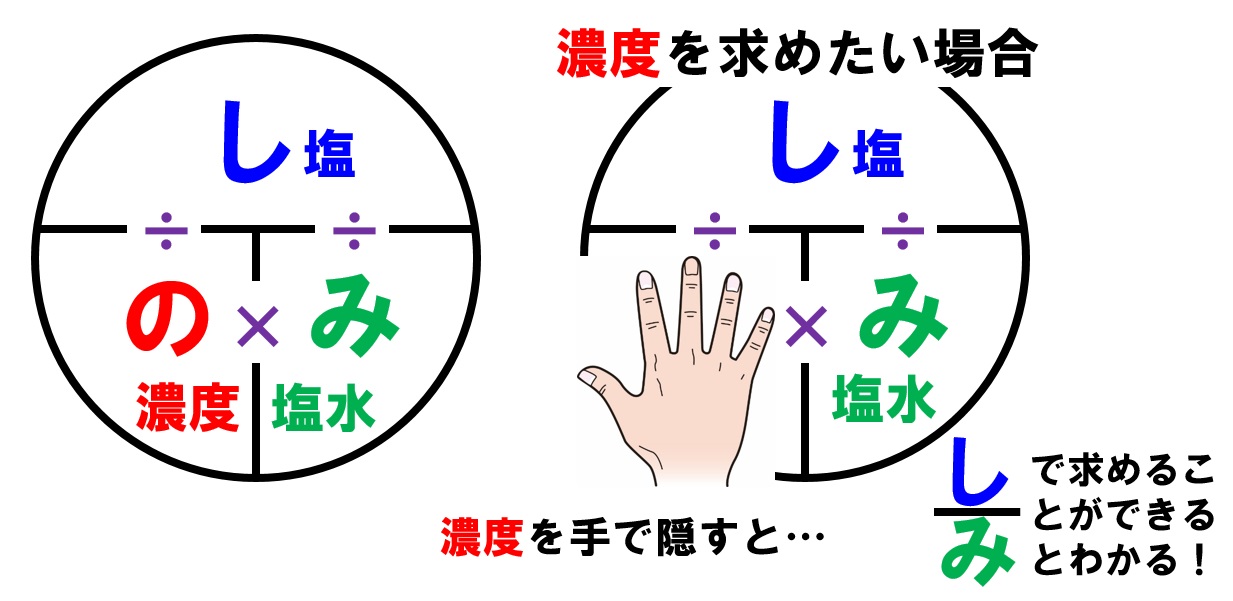
しわよ で覚える質量パーセント濃度 中学テスト 入試対策ノート




これらの問題が分かりません 誰か教えてくださいm M Clear




モル 濃度 ピクチャー ニュース




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




4 6 溶液の濃度 おのれー Note



10倍に薄めてない食酢中の質量パーセント濃度はいくらか 食酢 Yahoo 知恵袋
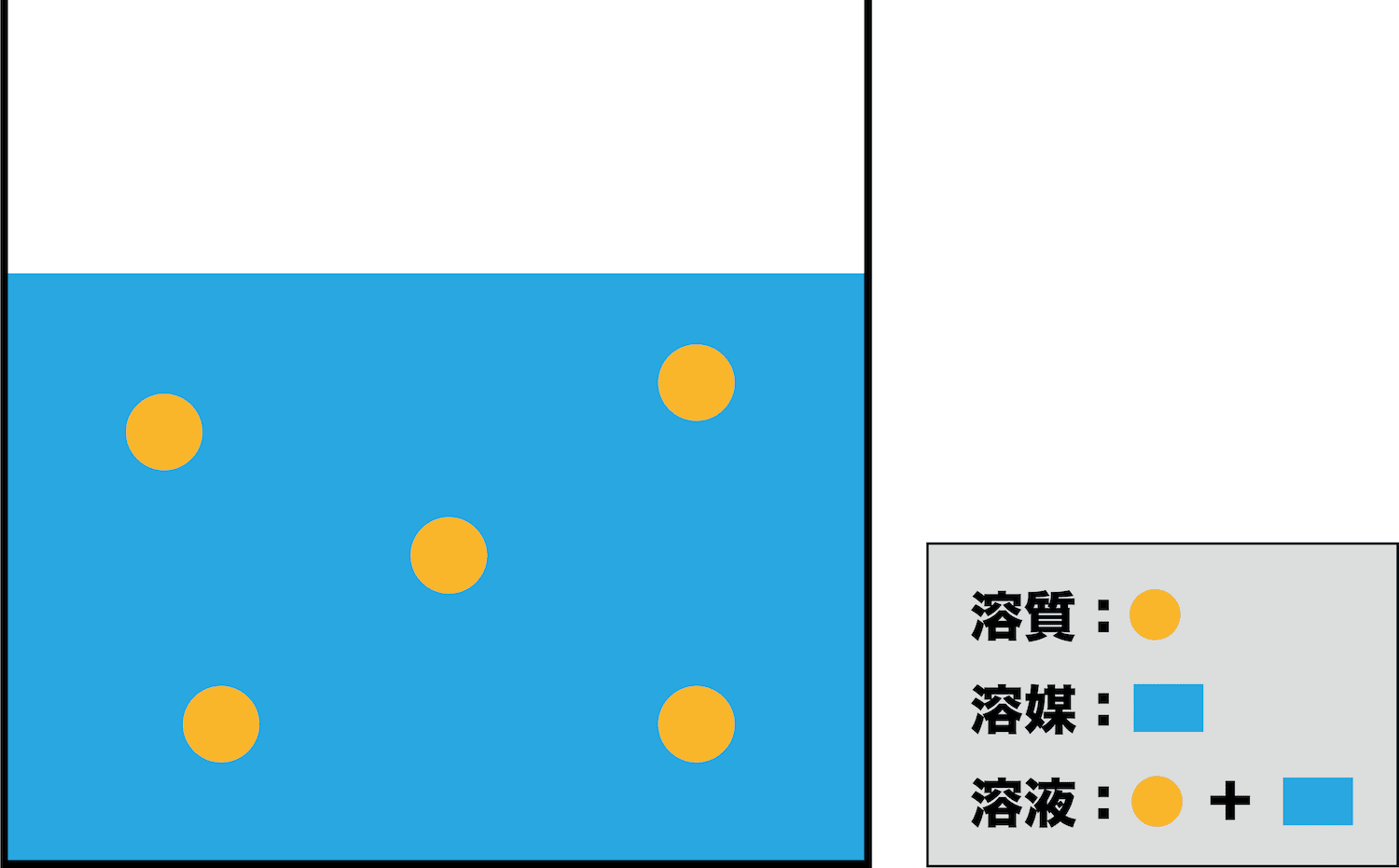



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




4 6 溶液の濃度 おのれー Note




高校化学基礎 硫酸とモル濃度 映像授業のtry It トライイット




至急 質量パーセント濃度が98 の濃硫酸の密度は1 8g Cm3である この 高校 教えて Goo




モル濃度と質量パーセント濃度 Youtube



3 3 密度から質量パーセント濃度を求める問題テストの問題だったものですが Yahoo 知恵袋
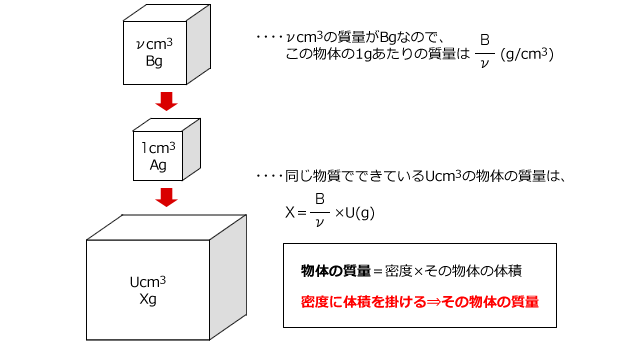



化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム



化学基礎モル濃度の計算問題です 類題3 1 質量パーセント濃度が Yahoo 知恵袋




モル濃度1 0mol Lの過酸化水素水 密度1 2g Cm の質量パーセント濃度 Clear




解説を見ても分かりませんでした 詳しく教えてください Clear




質量パーセント濃度の求め方 問題を使ってかんたんに解説するぞ 中学数学 理科の学習まとめサイト
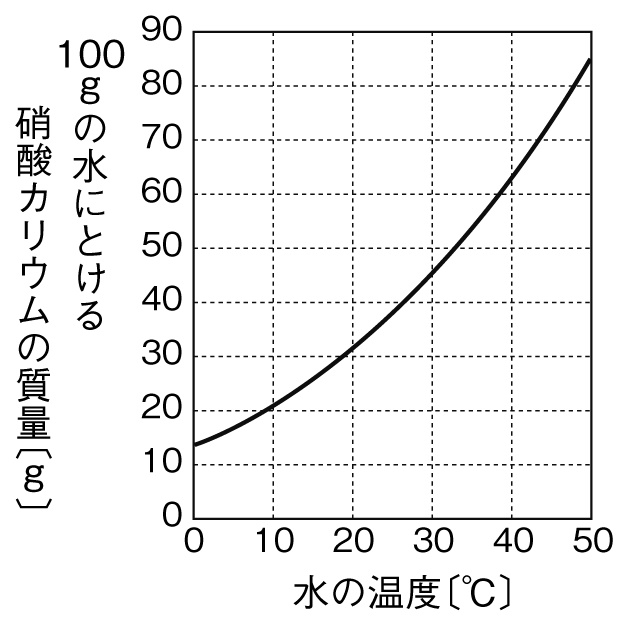



定期テスト対策問題 質量パーセント濃度の計算演習問題 Examee



1




公式がわかれば 文字式計算の問題も 化学がちょっとだけ好きな社労士



質量パーセント濃度 モル濃度 密度の関係が全然分かりません 密度が関 Yahoo 知恵袋




質量パーセント濃度63 の濃硝酸hno3 密度1 4 Cm 3 のモル濃度は何mol Clear



Mol濃度 質量パーセント濃度 質量モル濃度の相互変換の仕方のコツ




モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine




高校化学基礎 硫酸とモル濃度 映像授業のtry It トライイット



化学 Mol濃度 質量パーセント濃度 Youtube




西村能一 科学の名著50冊が1冊でざっと学べる Kadokawa Twitterren 化学計算問題 4 濃度 Mol L Mol Kgを求める 水酸化ナトリウム25gを水100gに溶解させた溶液の密度が1 2 G Cm3であった 1 この水溶液の質量パーセント濃度は何 か 2 この水溶液




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット




7 365 12g Cm3 Hc C1 Left Descubre Como Resolverlo En Qanda




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく



気体の溶解度




例題3の解き方を教えてください ちなみに 答えは 1 15mol L Clear
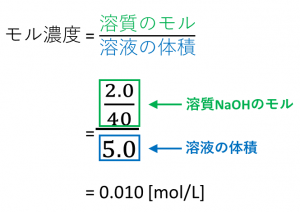



モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine



モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




090g Cm3 Descubre Como Resolverlo En Qanda



Search Q Ab E8 E9 87 8f Tbm Isch



モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




6 7 モル濃度と密度から質量パーセント濃度を計算します 1lあったとしたら と仮定すれば あとは簡単です プレテスト化学基礎 第3問 問3 Youtube




高校理論化学 食酢中の酢酸のモル濃度と質量パーセント濃度 受験の月



質量 パーセント 濃度 求め 方



Q Tbn And9gcrw0sr8fxbtv6xpolr16pkuz71aw74l2xddhh9xvrhoimgmlj L Usqp Cau



質量パーセント濃度 簡単な公式で覚えよう おときち副塾長 電脳空間学習塾かもん Youtube




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




中1 理科 中1 32 質量パーセント濃度 Youtube



化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット




考察がわからないので教えてください Clear



質量パーセント濃度28 密度1 2g Cm3の希硫酸について 2 Yahoo 知恵袋



中1理科 濃度の計算特訓 混ぜ合わせの濃度計算まで Pikuu




西村能一 科学の名著50冊が1冊でざっと学べる Kadokawa 化学計算問題 4 濃度 Mol L Mol Kgを求める 水酸化ナトリウム25gを水100gに溶解させた溶液の密度が1 2 G Cm3であった 1 この水溶液の質量パーセント濃度は何 か 2 この水溶液




質量パーセント濃度の計算問題集 基本編 Menon Network



1




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ




برچسب 質量パーセント濃度 در توییتر




理科 中1 27 質量パーセント濃度 Youtube




エレガント質量 パーセント 濃度 最高のぬりえ




5 98 Descubre Como Resolverlo En Qanda




2 10 050m0l 1l 100 M Descubre Como Resolverlo En Qanda




中1 理科 質量パーセント濃度の計算 P塾




質量パーセント濃度の計算問題集 応用編 Menon Network



Http Www Maruoka J Ed Jp Pdf Rika2kotae Pdf




質量パーセント濃度 密度で求められるのは質量ですか Clear




センター試験の密度の問題 とっても簡単 化学がちょっとだけ好きな社労士




高校化学 質量パーセント濃度をモル濃度へ変える方法 Youtube



モル濃度 質量パーセント濃度 質量モル濃度 濃度計算のコツも解説 受験メモ




1 M P Lihat Cara Penyelesaian Di Qanda



0 件のコメント:
コメントを投稿